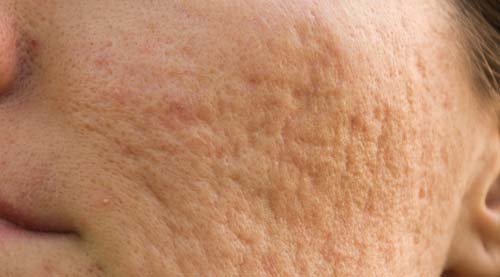
Amerykańska Agencja ds. Żywności i Leków (The U.S. Food and Drug Administration) po raz pierwszy zatwierdziła wypełniacz w leczeniu blizn potrądzikowych. To jeden z najczęstszych defektów skórnych. Tylko w Stanach Zjednoczonych problem ten dotyczy około 40-50 mln osób.
Pod koniec 2014 r. FDA po raz pierwszy zatwierdziła filler (Bellafill) we wskazaniu: leczenie głębokich, potrądzikowych blizn na policzkach u pacjentów powyżej 21 roku życia. Materiał ten od 2006 roku był oficjalnie stosowany jako wypełniacz do korekcji fałd nosowo-wargowych. Do końca stycznia ma wystartować sprzedaż produktu w nowym wskazaniu w Stanach Zjednoczonych.
Kluczowym składnikiem preparatu jest odzwierzęcy kolagen. Po wstrzyknięciu wypełniacz ma za zadanie podnieść dno blizny oraz wygładzić ją, tak aby zrównała się z poziomem zdrowej skóry i stała się niewidoczna. Badanie kliniczne fillera przeprowadzono na próbie 150 pacjentów z bliznami potrądzikowymi. Wyniki Bellafillu porównywano z grupą osób, które otrzymywały placebo. Zaobserwowano znaczącą poprawę u pacjentów, którzy poddali się leczeniu, trwającemu co najmniej przez rok.
Jak pisze agencja Reuters dostępne obecnie metody leczenia blizn potrądzikowych nie spełniają oczekiwań wielu osób dotkniętych tym problemem. Tymczasem badania kliniczne nad Bellafillem, które wykonano na potrzeby FDA pokazują, że może to być istotna alternatywa.
– Do tej pory w leczeniu blizn potrądzikowych stosowane były wielozabiegowe terapie laserowe, czy iniekcje, jednak ich skuteczność i trwałość była ograniczona oraz obarczona ryzykiem powikłań – komentowała dla agencji Reuters dr Ava Shamban z wydziału dermatologii klinicznej na Uniwersytecie Kalifornijskim (UCLA), która była zaangażowana w badania kliniczne nad Bellafillem.
Dla Reuters Health sprawę nowego wskazania dla fillera komentował też amerykański analityk z firmy Sanford C. Bernstein – Aaron Gal, powiązany z Allerganem (producentem m. in. Botoxu). Według niego jest to niszowy produkt jednak nowe wskazanie sprawia, że może być interesujący.
Z drugiej strony wątpił w marketingowy potencjał takiego nowego zastosowania wypełniacza. Zwracał też uwagę, że wypełnianie blizn jakąkolwiek substancją może nie wytrzymać próby czasu, ze względu na zmiany elastyczności skóry z wiekiem.
Źródło: rynekestetyczny.pl/FDA, Reuters Health